熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
三叉神經痛是最嚴重的神經病理性疼痛形式,其主要表現為單側口面部三叉神經支配區域內反復發作的、短暫劇烈的電擊或刀割樣劇烈疼痛,常由輕觸、說話、洗臉等日常無害行為觸發。目前,血管壓迫尚未進入腦橋的三叉神經根并導致壓迫位置局部脫髓鞘被認為是臨床上最常見的經典型三叉神經痛的關鍵病理環節。相應地,三叉神經根微血管減壓術對經典型三叉神經痛具有一定程度的治療效果。然而,有些具有典型癥狀的三叉神經痛患者要么微血管減壓術療效不佳,要么在其三叉神經根區域并不存在確切的脫髓鞘病變。因此,很有可能是其他區域的神經病變導致此類三叉神經痛。
既往臨床研究觀察到,繼發于多發硬化或者腦橋缺血梗死的三叉神經痛患者很可能是由腦橋三叉神經束(pontine trigeminal tract,PTT)區域的脫髓鞘病變引起的。最近研究進一步發現,很大一部分微血管減壓術療效不佳的三叉神經痛患者全腦范圍內僅僅在腦橋三叉神經束區域出現脫髓鞘病變。與此同時,腦橋三叉神經束脫髓鞘病變被發現可以預測微血管減壓術治療三叉神經痛是否有效。這些臨床證據提示,除了常見的三叉神經根脫髓鞘,腦橋三叉神經束脫髓鞘同樣可能導致具有典型病癥的三叉神經痛。然而,目前尚未有臨床隊列或動物模型研究進一步明確這種臨床推測。
溶血磷脂酰膽堿(lysophosphatidylcholine,LPC)常被用于建立中樞神經系統局部脫髓鞘模型。因此,本研究擬利用成年大鼠腦橋三叉神經束LPC的腦立體定位微量注射,建立成年大鼠腦橋三叉神經束局部脫髓鞘模型,通過行為學和藥理學檢測腦橋三叉神經束局部脫髓鞘能否在成年大鼠上誘發三叉神經痛樣行為,從而明確腦橋三叉神經束脫髓鞘可以誘發三叉神經痛。本研究結果將為三叉神經痛的基礎研究和臨床診療奠定一定的基礎。
1材料與方法
1.1實驗動物
6~7周齡健康清潔級雄性SD大鼠,體質量200~220 g,購自成都達碩實驗動物有限公司。大鼠飼養于12/12 h(光照/黑暗)環境中,環境溫度控制在(22±1)℃,食水充足且可自由獲得。待外購動物適應本實驗環境且體質量達到250~270 g時開始實驗。以下有關動物的操作流程嚴格遵守四川大學實驗動物福利和倫理相關規定,并盡可能減少實驗動物的痛苦,降低大鼠使用量。
1.2主要試劑
LPC購自美國Sigma公司;FluoroMyelin Red髓鞘熒光染料購自美國Invitrogen公司;抗熒光衰減封片劑、卡馬西平購自北京索萊寶生物科技有限公司;異氟烷購自深圳瑞沃德生命科技有限公司;羥丙基-β-環糊精購自上海愛必信生物科技有限公司。
1.3實驗器材
小動物麻醉系統購自南京卡爾文生物科技有限公司;左臂單臂數顯型腦立體定位儀、玻璃微電極注射泵購自深圳瑞沃德生命科技有限公司;玻璃微電極購自丹麥Unisense公司;von Frey纖維絲套件購自美國Danmic Global公司;Air-puff控制系統購自日本MUSASHI公司;IX-83型倒置熒光顯微鏡購自日本Olympus公司;CM3050型冷凍切片機購自德國Leica公司。
1.4.1腦橋三叉神經束垂直型腦立體定位微量注射
用異氟烷麻醉大鼠后,將大鼠固定于腦立體定位儀。頭部剃毛,從大鼠頭部中縫處剪開皮膚,暴露術野。參照Wistar大鼠腦立體定位MRI圖譜,以Bregma為坐標原點,在其前后徑(anterior-posterior,AP):-9.86 mm;內外徑(medial-lateral,ML):2.75、2.85、2.95、3.05、3.25 mm處的顱骨表面鉆1個小孔,使玻璃微電極垂直進針8.50 mm,停留1 min后以250 nL/min的速度注射20 nL藍墨水,注射完成后留針5 min,緩慢升起電極。縫合頭皮創口并消毒,取下動物待其恢復清醒后放回飼養籠。
1.4.2腦橋三叉神經束傾斜型腦立體定位微量注射
大鼠腦橋三叉神經束ML范圍較窄(約0.5 mm),背腹徑(dorsal-ventral,DV)范圍相對寬厚(約1.8 mm),且在冠狀面上呈傾斜弧形(圖1),使得垂直型腦立體定位精準微量注射難度較大,故本研究擬進行傾斜型腦立體定位微量注射,以增加微量注射容錯率和成功率。動物準備如前所述,在AP-9.86 mm和ML 0 mm處的顱骨表面鉆1個小孔,使玻璃微電極左傾斜18°進針9.22 mm,停留1 min后以250 nL/min的速度注射20 nL藍墨水或者相應劑量的LPC或Vehicle,注射完成后留針5 min,緩慢升起電極。縫合頭皮創口并消毒,取下動物待其恢復清醒后放回飼養籠。
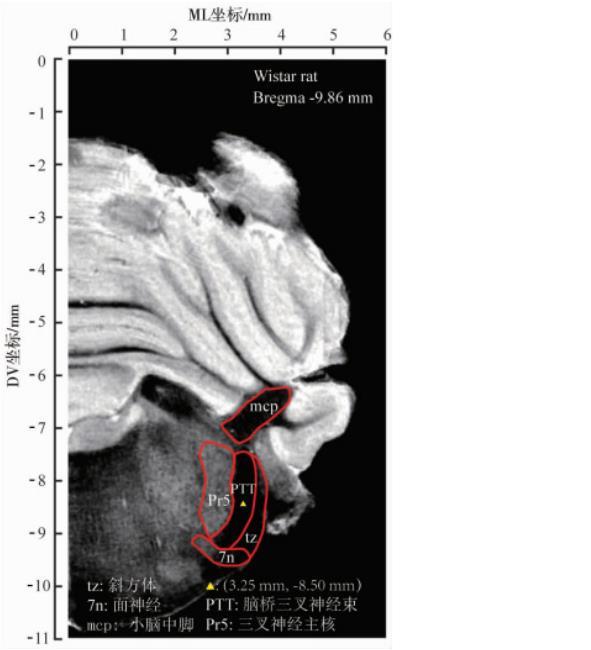
圖1 Wistar大鼠腦橋三叉神經束MRI示意圖
2結果
2.1成年大鼠腦橋三叉神經束局部脫髓鞘模型的建立
垂直型腦立體定位微量注射實驗結果表明,AP-9.86 mm、ML 2.85 mm、DV-8.50 mm是250~270 g體質量的成年雄性SD大鼠腦橋三叉神經束微量注射較為理想的腦立體定位坐標(圖2A)。傾斜型腦立體定位微量注射實驗結果顯示,于AP-9.86 mm、ML 0 mm和DV 0 mm處,將玻璃微電極左側傾斜18°下行9.22 mm,可使其穩定可靠地定位于腦橋三叉神經束內部(AP-9.86 mm、ML 2.85 mm、DV-8.77 mm;圖2B、C)。髓鞘熒光染色結果顯示,250 nL的1%LPC即可引起局限于腦橋三叉神經束內的明顯脫髓鞘;而更高劑量(500和1 000 nL)的LPC則引發腦橋三叉神經束區域大范圍以及腦橋三叉神經束區域外的嚴重脫髓鞘,且造成腦橋三叉神經束區域內溶脹性空洞等嚴重組織結構破壞(圖2D)。結果表明,1%LPC導致成年大鼠腦橋三叉神經束局部脫髓鞘的最佳劑量為250 nL。
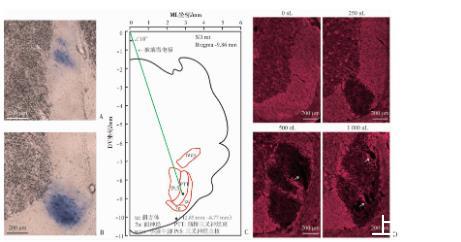
A:腦橋三叉神經束立體定位垂直注射藍墨水(ML 2.85 mm)分布區域(n=3);B:腦橋三叉神經束立體定位傾斜注射藍墨水分布區域(n=3);C:SD大鼠腦橋三叉神經束立體定位傾斜注射路徑示意圖;D:不同劑量1%LPC傾斜注射腦橋三叉神經束后第7天脫髓鞘情況白色箭頭:示空洞
圖2成年大鼠腦橋三叉神經束局部脫髓鞘模型的建立
3.結論
結合既往基礎和臨床研究,本研究結果進一步提示,廣泛分布于三叉神經傳入纖維通路的脫髓鞘病變是三叉神經痛發病的核心通用機制。此推斷有以下2方面的意義。一方面,三叉神經痛目前的治療要么通過以卡馬西平為代表的電壓門控鈉通道抑制劑減弱脫髓鞘神經元的異常興奮,要么采用侵入性或損毀性的手術治療解除血管神經壓迫或者破壞三叉神經感覺傳入;然而三叉神經痛目前的治療效果皆差強人意。臨床隊列研究發現,微血管減壓術是通過促進髓鞘再生實現對三叉神經痛的治療。因此,可以開發靶向促進髓鞘再生的治療手段,單獨或者聯合現有治療手段,以期提高三叉神經痛的治療效果和質量。另一方面,不同位置和不同性質的脫髓鞘病變導致的三叉神經痛雖然臨床癥狀差別不大,但是接受同一治療方案的效果卻存在很大差異。因此,三叉神經痛臨床實踐中需要擴大影像檢查范圍從三叉神經根至整個三叉神經傳入纖維通路,以便精確判斷脫髓鞘病變位置,進而選擇合理的治療方式,實現三叉神經痛的精準治療,提高該疾病的診療質量。
綜上所述,本研究表明,除了三叉神經根脫髓鞘,腦橋三叉神經束脫髓鞘同樣可以誘發三叉神經痛。該研究結果將為三叉神經痛的機制/治療研究和臨床精準治療奠定一定的基礎。
 相關新聞
相關新聞