熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
電化學技術為廢水處理和化學合成提供了一種清潔而強大的工具。(生物)電化學系統通過向微生物生長的電極施加電勢來催化(微生物)轉化。微生物將施加的能量直接用作電子或間接用作氫,氫在陰極由電子和質子形成。微電極傳感器有一個薄的尖端(低至1μm),這使得測量具有與尖端尺寸相同的空間分辨率。傳感器可以沿著輪廓軸移動來測量梯度。微電極傳感器已經應用于許多不同的領域,包括生物化學,植物科學,微生物學和生物醫學,但是它們在電化學系統中的應用仍然有限。微電極傳感器在電化學系統中的應用有望通過電流型微傳感器的應用而變得合適,電流型微傳感器測量由微電極表面上的氧化還原反應產生的電流信號。
在(生物)電化學系統中使用電位微電極分析局部梯度時,需要解決電場干擾問題,解決該問題的最佳方法是盡量減小傳感電極和參比電極之間的距離。在定制的傳感器中,參比電極和測量電極內置在同一個傳感器中,并與導電液體相連。雖然這給出了可靠的結果,但較厚的微傳感器尖端不允許傳感器移動超過600μm的距離而不穿透生物膜上毫米寬的孔。短距離足以測量2D電極上的生物膜內部,但不能用于測量通常用于生物陽極或生物陰極中的幾毫米或甚至厘米厚的3D多孔電極內部。在本研究中,提出使用一種微電極感測器(unisense)應用于開發了(生物)電化學系統來測量電解液中的梯度,并首次測量整個多孔3D電極。方法開發包括三個步驟。首先設計了一個反應器,其關鍵功能允許在幾厘米范圍內進行微輪廓測量,保持厭氧條件和10 L/h的連續無泄漏液體電解質再循環。實用技巧和方案以便于使用和小心處理微傳感器。第二,反應器設計用于顯示H的微觀分布。第三,提出并驗證了一種克服電位微傳感器測量過程中電場干擾的校正方法,利用該方法,電位微傳感器最終可以應用于(生物)電化學系統中的梯度精確測量,即使在高電流(?10 kA/m)下也是如此)。校正方法用于顯示電場電位、ORP和pH的梯度分布。研究中的分布顯示電極表面的整體條件和局部條件之間存在顯著差異,這突出了所提出的方法的重要性及其在傳質研究中的可能應用。
Unisense微電極系統的應用
將實驗臺(LS18)、微操作器(MM33-2)、電機驅動微操作器平臺(MMS)和電機控制器(MC-232)組合在一起,以精確操作微傳感器(Unisense)。H2微電極傳感器(H2-50),pH微電極(pH-50),氧化還原電位微電極(RD-50),參比微電極(REF-100)和電位電極(EP-100)用于微成型,所有尖端尺寸均為40-60μm(全部來自Unisense,在宏觀下確定相對傳感器長度,以能夠在圖中組合不同的傳感器測量。對于電位微傳感器,將兩個外部毛細管安裝在5mm以上和反應器中陰極下方7mm處,毛細管填充有凝膠化的3M KCl,并通過填充有液體3M KCl的管道連接到Ag/AgCl參比電極。
實驗結果
unisense微傳感器在電化學系統中測量梯度的成功應用。反應器的測量井垂直于剖析方向,允許剖析電解液無泄漏再循環條件。所提供的手冊和視頻說明將幫助未來的用戶應用這種方法。分析了電解質中的局部H2、電勢、pH和ORP,并首次在整個多孔電極中進行了分析。對于電位型微傳感器,局部電場電位校正是一種可靠的校正電場擾動的方法。這些傳感器的應用可以擴展到電化學系統中生物膜梯度和局部反應器條件的研究。
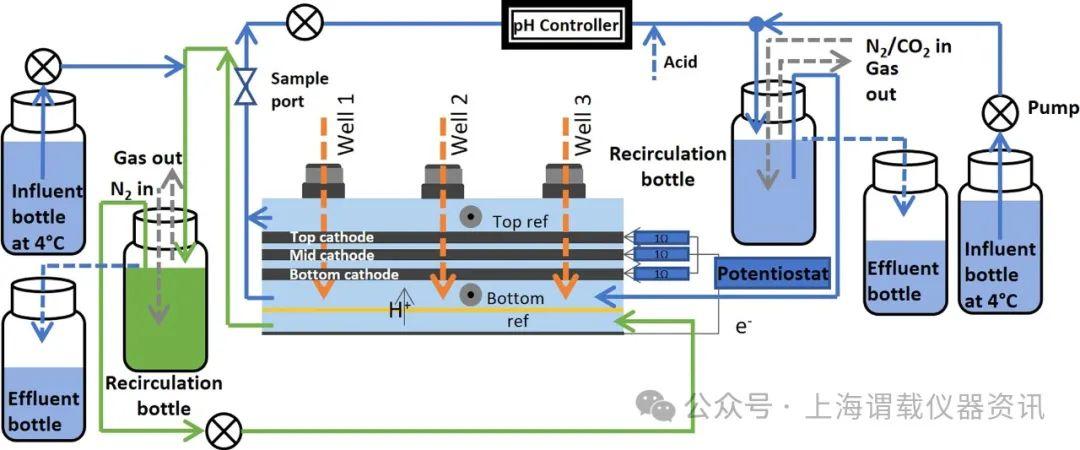
圖1、帶有再循環、流入液、流出液和pH值控制的電化學槽的設置。陽極電解液再循環以綠色顯示,便于查看。
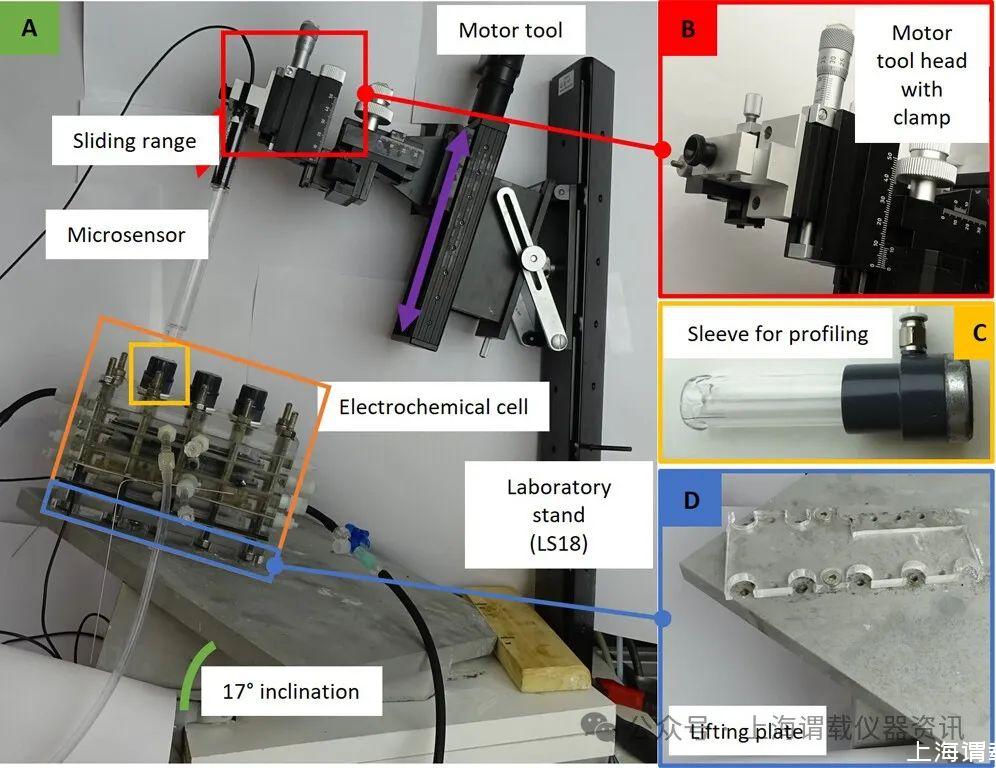
圖2、在(生物)電化學反應器中制作微輪廓的裝置。將電化學反應器放置在升降板(D)上,該升降板以17°傾角(A)連接到接地板上。為了制作微輪廓,將微傳感器放置在馬達工具頭夾(B)中,并通過套筒(C)進入反應器。為了測量微剖面圖,陰極電解液循環被短暫停止,以"套管"(圖二C)進入微傳感器。用硅脂潤滑微傳感器頸部,以確保頸部和套管之間的水密密封。硅脂允許電解質無泄漏地移動傳感器。在將微傳感器固定在套管中之后,再次打開再循環,并且可以形成微剖面,在此期間,使用電動工具(默認速度和加速度為1000μm/s和1000μm/s)將微電極傳感器取下,步長為100μm)(圖二B)刺穿石墨電極,并通過陰極層形成梯度,直至插入到電池內的膜。
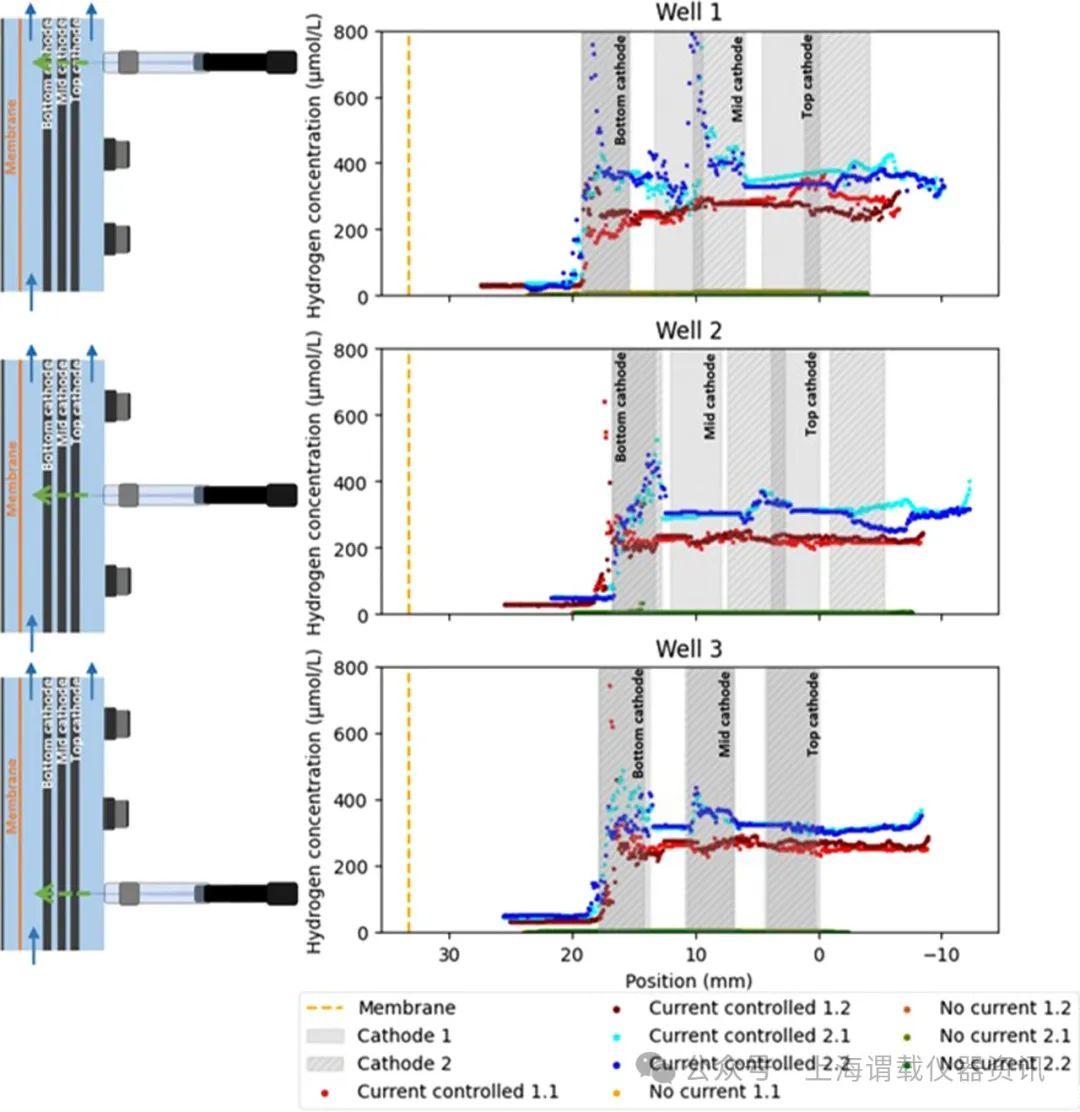
圖3、在-200 mA和無電流條件下,兩個電化學反應器(1和2)內氫濃度隨距離變化的曲線圖,左圖為反應器示意圖,每個反應器(1和2)繪制了兩次曲線圖。在沒有電流施加到電化學電池的情況下,沒有檢測到氫氣。在施加電流的情況下,最靠近反電極的陰極電解液中的氫濃度低(圖三20-25mm的距離),并且在最靠近反電極的陰極處最高。

圖4、pH微傳感器測量(A)在不同的陰極電流幅值下,本體pH值與由放置在陰極室的本體入口點處的pH微傳感器報告的pH值之間的偏差,相對于頂部固定的參比物測量pH信號。(B,C)在-50 mA下運行的電化學反應器內pH值隨距離變化的曲線。相對于頂部固定的參比電極測量pH值,相對于底部固定的參比電極測量pH值兩次。(B,黑色)和底部(B,黃色)參比電極用EP頂部校正(B,綠色)和底部(B,淺藍色)參考曲線,以獲得校正的pH曲線還用開孔測量pH曲線(C,藍色)。在形成pH頂部參考曲線之后,立即將pH微傳感器尖端放置在底部參考電極旁邊,并記錄7分鐘(C,黃色十字)。當沒有電流施加到系統時,在再循環pH和微傳感器pH(圖六A)。在施加電流的情況下,pH微傳感器報告的pH值低于再循環pH值。這種偏移隨著電流的增加而增加,呈半線性趨勢。在-100 mA或更負的電流值下,pH微傳感器甚至報告負pH值。因此,信號與施加電流的再循環pH值嚴重偏離。
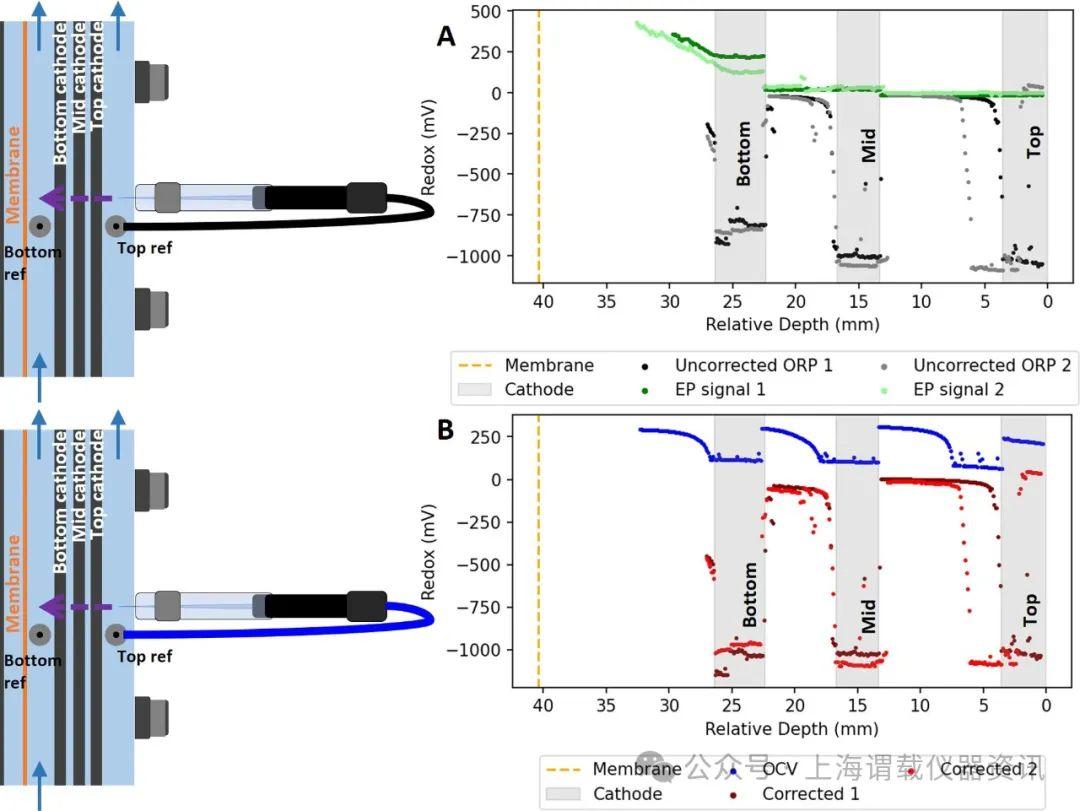
圖5、氧化還原電位的重復曲線在-200 mA下運行的電化學反應器內的距離上的氧化還原電位(ORP)。氧化還原電位是相對于頂部固定的參比電極測量的。氧化還原電位測量的原始數據是相對于頂部參比電極測量的。(A,黑色和灰色)使用EP頂部參考輪廓進行校正(A,綠色)以獲得校正的ORP曲線(B,紅色)。用開池電壓測量ORP分布在不同的反應器(1和2)中進行兩次重復測量,并且出于觀察的目的僅示出了來自一個反應器(1)的陰極位置。
結論與展望
本研究開發了一種基于使用微傳感器測量pH和H2的技術梯度在微生物電合成。使用三維電極(生物)電化學系統可能導致從本體條件到電極的梯度的出現。由于這些梯度(例如,關于pH和反應物/產物濃度)決定電極的性能,因此能夠準確地測量它們是至關重要的。除了這些參數之外,還測定了電解液中和整個3D多孔電極中的局部氧化還原電位和電場電位。關鍵是認識到電場的存在干擾了通過電位型微傳感器(unisense)獲得的測量結果。為了克服對pH測量的干擾,驗證了一種用電位微傳感器測量系統(unisense)局部電場來校正信號的方法,該方法為電極設計、反應器工程、電活性生物膜梯度測量以及(生物)電化學系統三維多孔電極內部和周圍的流體動力學研究提供了有用的工具。