熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
活體伏安法是將微電極直接插入大腦特定部位,實現腦內生理活性物質的活體實時分析的電化學分析方法。因其所用微電極尺寸小,可置入腦組織,分析時空分辨率高,活體伏安法在腦神經化學過程的研究中備受關注。
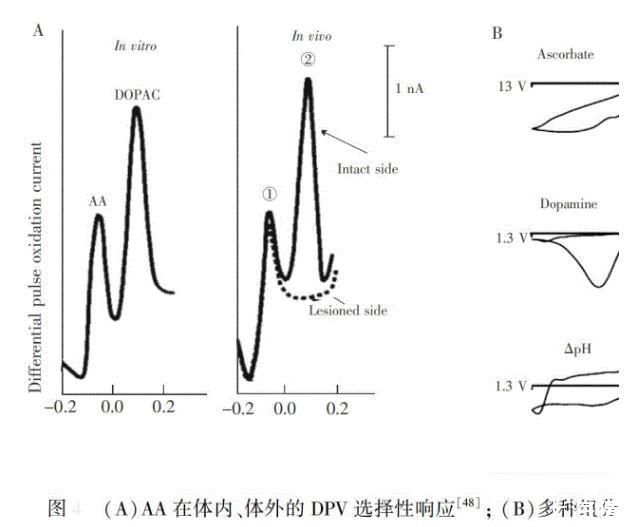
Adams等于1972年第一次將碳糊電極(直徑約300μm)植入大鼠腦內,并獲得了腦內第一張循環伏安圖,并猜測所獲得的伏安信號為AA的氧化峰。用同樣的方法,O'Neill等通過腦區微注射和腹腔注射AA,增加了伏安信號,Brazell等通過向腦區注射AA選擇性氧化酶(Ascorbate oxidase,AAOx),證實了獲得的伏安信號為AA,并用該方法測定了不同腦區和微注射谷氨酸時AA的變化。然而,碳糊電極直徑太大,碳纖維電極(CFE,5~7μm)具有較高空間分辨率和生物兼容性等性能,因此,越來越多研究開始關注CFE,并發展了許多檢測AA的方法。Gonon等第一次對CFE進行處理,用DPV法實現了腦內AA的選擇性分析。Heien等通過快速掃描循環伏安法(Fast scan cyclic voltammetry,FSCV)和主成分回歸分析對FSCV數據進行了多組分分析,可同時測定AA、5 HT、DA、DOPAC、pH值的實時變化(。
如前所述,對電極表面進行合理的功能化,是實現AA選擇性分析的有效策略。第一次在電極表面修飾CNT,實現了AA的活體檢測。AA在CNT修飾的CFE上在0.0 V左右達到穩態電流,說明修飾在CFE上的CNT對AA具有很好的電化學催化作用。此外,DA、尿酸和5 HT這些腦內神經化學物質的氧化電位都比AA在CNT修飾的CFE氧化電位正,因此不干擾AA的電化學分析。他們通過多壁碳納米管(Multiwalled carbon nanotube,MWNT)修飾的CFE,用DPV的方法檢測鼠腦細胞間液中AA的濃度約為(0.20±0.05)mmol/L。他們通過向電極附近注入AAOx,證明MWNT修飾的CFE電極對AA具有很好的選擇性。
由于CNT修飾CFE的技術在神經科研領域的研究較難,且電極制備的可重復性有待進一步提高,Xiang等制備了陣列碳納米管覆蓋的碳纖維微電極(Vertically aligned carbon nanotube sheathed carbon fiber,VACNT CFE),大大簡化了碳納米管微電極的制備方法,避免了手工滴涂修飾CNT引起的電極性能差異,以及繁雜修飾步驟。CFE(A)和VACNT CFE(B)的掃描電鏡圖,CNT均勻生長在CFE表面,在稀H2SO4溶液中電化學預處理,得到的VACNT CFE對AA的響應與裸CFE相似,然而,VACNT CFE在NaOH溶液中電化學活化后,表現出對AA良好的電催化性能,降低了AA氧化的過電位,并增大了其電流響應,這些實驗結果證明了CNT的端口碳對AA具有良好的催化性能。VACNT CFE對AA的分析呈現出良好的選擇性和線性關系,并可觀察到灌注谷氨酸所引起的AA釋放,實時監測了AA和谷氨酸的異相交換行為。
在CFE表面垂直生長CNT方法可用于腦內AA測定,雖然該電極制備方法可避免人工修飾引起的一系列問題,但是該方法復雜,不利于大量制備電極。為進一步簡化CNT電極的制備,Xiao等發展了一種可控且重現性極高的電泳沉積SWNT修飾電極的方法,電泳的方法可非常簡單地將酸化處理的SWNT沉積到CFE表面,該電極對AA的電化學氧化表現出良好的催化作用,重現性高。
重要的是,檢測AA時,CNT修飾的CFE比電化學處理的CFE具有更好的穩定性,因此有利于研究腦科學與AA相關的生理或者病理過程中AA變化。如擴散性抑制(Spreading depression,SD)是一種在腦內神經細胞去極化,隨后受到抑制并類似去極化波在神經及膠質細胞間進行傳播的現象。SD發病過程與偏頭痛、癲癇發病過程非常相似。因此SD發病過程中機理的研究,對于相關疾病的發病機制的研究和治療都有重要的參考意義。Xiao等用SWNT修飾的CFE測定了鼠腦皮層由電刺激引發的SD過程中AA的濃度動態變化。利用給予局部注射AAOx和改變施加電位的方式,進一步驗證記錄到的電流的變化是由SD導致胞外AA濃度變化引起的。為進一步理解SD過程中AA釋放的機理,局部注射NMDA受體拮抗劑地佐環平(MK 801)阻斷谷氨酸依賴的SD的傳播,并可抑制SD過程中AA的釋放,進一步證明了AA的釋放受SD過程中谷氨酸的調節。為了探索AA的釋放是否是由于谷氨酸異相交換引起的,采用D,L蘇式β芐氧基天冬氨酸(D,L TBOA)進行干預,大鼠給予D,L TBOA后,發現電刺激AA的釋放并未被抑制。因此,報道認為SD過程中AA釋放并不是谷氨酸的異相交換引起的,可能與SD過程中細胞水腫密切相關。
比率型電分析引入內參比氧化還原電對,使用待分析物和內參比的電流響應對分析物進行分析,可克服復雜體系的基底效應。Tian研究組首次提出比率型電分析策略,并將CNT紡成碳纖維絲,制備得到CNT纖維(Carbon nanotube fiber,CNF),實現了活體內比率型AA的分析檢測。AA在CNF上的氧化電位為50 mV,利用DPV技術,結合比率型電化學方法,對腦內的AA實現了選擇性分析,采用該方法觀察到到老年癡呆癥大鼠皮層、紋狀體和海馬3個腦區AA含量明顯低于正常大鼠。將硫瑾固定在炭黑修飾的CFE上,結合比率型電化學,用循環伏安法選擇性檢測聽皮層的AA,并觀察到水楊酸鈉引起的耳鳴過程中AA的變化。
同時記錄神經元的電活動信息以及腦內AA的動態變化可將神經細胞之間的信號傳遞與AA密切相關的神經調節過程聯系起來,從而深入理解腦生理和病理過程的信號轉導機制。Cheng等將SWNT修飾的CFE和毛細管玻璃微電極有效集成為雙通道微電極(Integrated dual mode microelectrode,IDMME),用CFE選擇性記錄AA,用玻璃管微電極記錄電生理信號,該雙通道微電極可獨立記錄化學和電信號,兩種信號之間沒有交叉干擾,并成功地用于原位連續監測大鼠腦缺血/再灌注過程中AA以及神經元細胞電活動的動態變化。
生物大分子在電極表面的吸附是活體原位分析AA面臨的另一個挑戰,因為腦內環境較復雜,不僅存在許多小分子干擾物質,還包含許多生物大分子(如脂質,蛋白質)。電極植入后腦內生物大分子會在電極表面吸附,導致電極檢測靈敏度下降,使得電極必須在活體檢測后進行校正,才能對活體數據進行分析。Liu等發現,用牛血清蛋白(Bovine serum albumin,BSA)處理后的CNT修飾CFE電極的活體檢測前校準曲線和活體檢測后校準曲線基本一致,從而巧妙地實現了活體前校準,克服了活體檢測過程中或者活體分析后微電極取出時電極斷裂無法校準的問題。
 相關新聞
相關新聞