熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
植入式生物電子學為實時和連續監測活體生理信號提供了前所未有的機會。大多數生物電子學采用薄膜襯底,如聚酰亞胺和聚二甲基硅氧烷,表現出高水平的柔性和可拉伸性。然而,這些薄膜的低透氣性和相對高的模量阻礙了長期的生物相容性。相比之下,在多孔基底上制造的器件具有高透氣性的優點,但圖案密度低。
創新點
香港理工大學Zijian Zheng和香港城市大學Xinge Yu課題組提出了一種晶圓尺度的高分辨率制造策略,用于超軟,可拉伸和高透氣性的液態金屬微電極(μLMEs)。通過光刻技術在4英寸彈性纖維氈上展示了2μm的圖案化能力,或高達~75,500個電極/cm2的超高密度μLME陣列。植入μLME陣列作為神經接口,對活體大鼠的皮質電圖信號進行高時空定位和干預。植入的μLMEs具有8個月以上的長期生物相容性。
文章解析
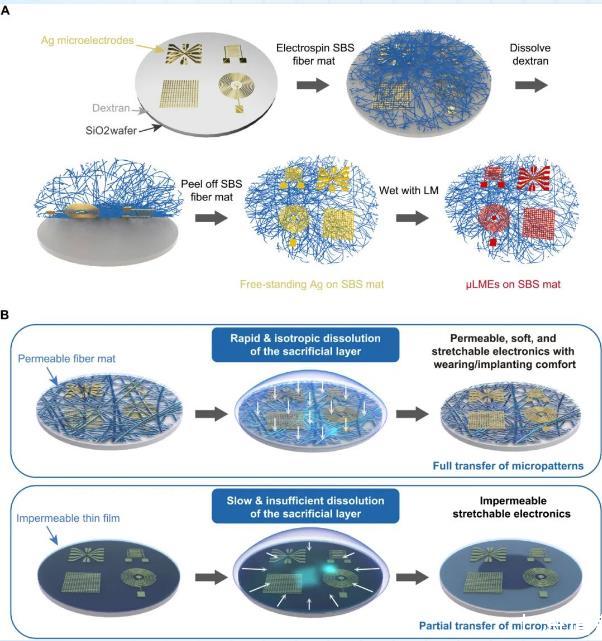
圖1:可拉伸和可滲透的液態金屬微電極(μLMEs)的制備過程。(A)μLMES制造過程的示意圖。(B)比較使用可滲透的纖維墊或不可滲透的薄膜對犧牲層的不同溶解過程影響示意圖。
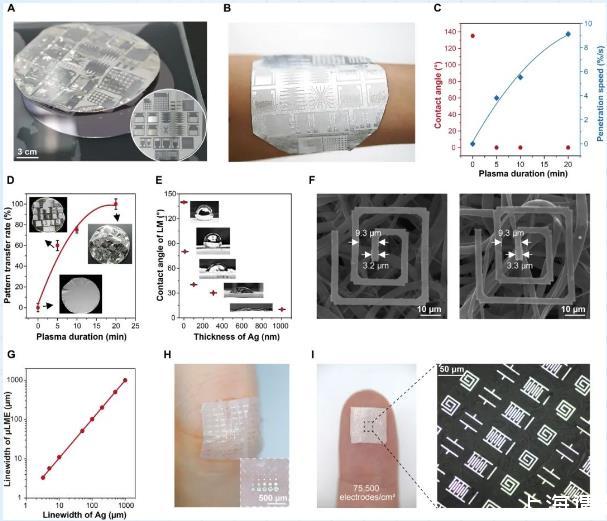
圖2:μLMEs結構示意圖。(A)銀微圖案從晶圓轉移到SBS纖維墊的圖像。插圖為轉移之前在晶圓上的圖案。(B)附著在人體手臂上的μLMEs的圖像(液態金屬負載量:10 mg/cm2)。(C)溶劑對犧牲層的接觸角和滲透速度以及(D)圖案轉移成功率與等離子體處理時間的函數。(E)LM在轉移銀層上的接觸角隨銀厚度的變化。(F)選擇性潤濕前后SBS纖維墊上電極的掃描電鏡圖像。(G)μLMEs的線寬與Ag電極的原始線寬的對應關系。(H,I)μLMEs高密度陣列的,陣列密度高達75500電極/cm2。
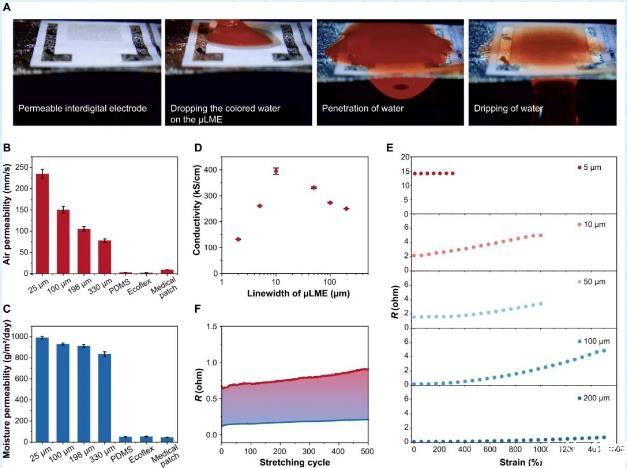
圖3:μLMEs的滲透性、導電性和拉伸性表征。(A)一個彩色水滴從μLMEs的一側滲透到另一側光學圖像。(B,C)μLMEs在不同厚度SBS纖維墊上以及其他生物電子學常用襯底,包括PDMS,Ecoflex和醫療貼片上的透氣性和透濕性表征。(D)不同線寬下μLMEs的電導率變化。(E)不同線寬μLMEs在不同拉伸應變下的電阻。(F)在1000%的大拉伸應變下μLMEs(線寬50μm)的循環電穩定性。
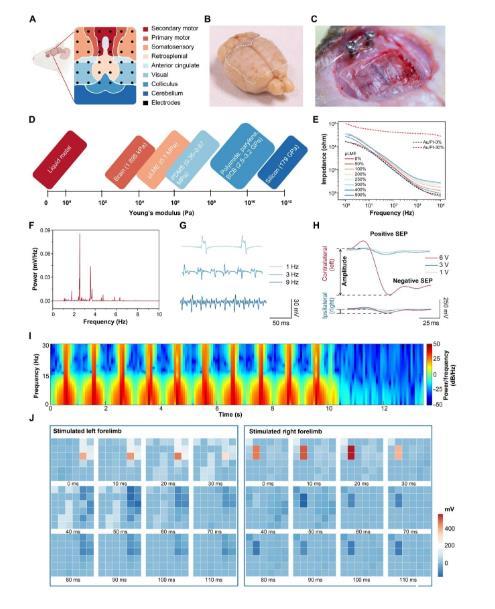
圖4:基于高密度μLMEs的神經電生理界面生物電子學表征。(A)基于μLMEs的ECoG陣列的示意圖和記錄的皮質子域。(B,C)μLME ECoG電極陣列(厚度25μm)在柔軟、彎曲和復雜的大腦皮層上適形附著的數字圖像。虛線表示μLME陣列的邊界。(D)μLMEs的楊氏模量與已經報道的ECoG生物電極材料的比較。(E)不同應變下μLMEs和Au/PI電極的體外電化學阻抗譜(EIS)表征。(F)活體大鼠睡眠狀態下體內神經信號的功率譜分析。(G)用μLMEs記錄不同頻率脈沖電壓電刺激下的體感誘發電位(SEPs)。(H)不同強度脈沖電壓電刺激下對側和同側體感覺皮質電位的比較。(I)對側體感覺皮層在10次強度為6 V、頻率為1 Hz的連續電刺激下的信號譜圖。(J)左右前肢電刺激下μLME陣列的時空特性研究。
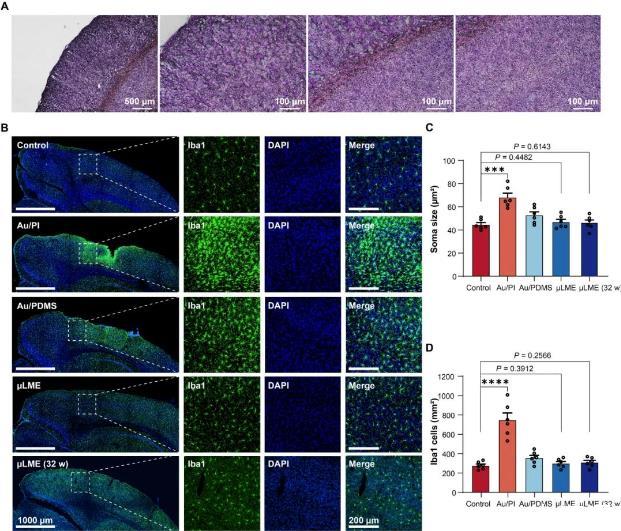
圖5:μLMEs用于慢性神經植入物的慢性(長期)生物相容性表征。(A)電極陣列植入2小時后染色腦切片的免疫組織學分析。(B)對照植入后2周,Au/PI電極、Au/PDMS電極、μLME電極和μLME電極,植入時間為32周(32w),免疫組化染色小膠質細胞(Iba1,綠色)和細胞核[4′,6-二氨基-2-苯基吲哚(DAPI),藍色]。左圖為低放大圖(比例尺=1000μm),右圖為高放大圖(比例尺=200μm)。(C)小膠質細胞胞體大小的統計分析(n=6)。Au/PI組(P=0.0002)和Au/PDMS組(P=0.0375)的小膠質細胞胞體大小與對照組相比顯著增加(雙向,非配對Student's t檢驗)。μLME組與對照組之間差異無統計學意義(植入后2周P=0.4482,植入后32周P=0.6143)。(D)總小膠質細胞數量的統計分析(n=6)。與對照組(雙向,未配對的學生t檢驗)相比,在AU/PI組(P<0.0001)和AU/PDMS組(P=0.0274)中發現了IBA1細胞的顯著增加。μLME組和對照組之間沒有發現顯著差異(植入后2周時P=0.3912,在植入后32周時P=0.2566)。
結論與展望
作者提出一種晶圓級高分辨液態金屬微電極(μLME)的制備方案,在超軟,可拉伸和高透氣性纖維墊上實現了每平方厘米75000個電極的圖案分辨率,這些μLME顯示出優異的機械柔性,當延伸至1000%應變時仍表現出出色導電性,以及在皮膚附著和植入測試中的生物相容性,并且可以用于腦皮層電信號的采集。這一方案為高密度,可集成,可植入的生物電子提供了解決思路。
 相關新聞
相關新聞