熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
癲癇在從出生窒息中恢復的新生兒中很常見,但人們普遍認為目前的藥物治療效果不佳,需要新的抗癲癇藥物。苯巴比妥(PhB)是新生兒癲癇發作的一線治療藥物,12包括由HIE引起的癲癇發作,但它在治療的前24小時內僅抑制40%–80%的新生兒癲癇發作。最近在出生窒息的大鼠模型中表明,癲癇發作是由窒息后腦pH值的恢復引發的。腦pH調節多種離子通道的功能,這些離子通道控制神經元興奮性和突觸信號傳導。這些通道以功能協同的方式響應pH值的變化,因此酸中毒抑制神經元興奮性和癲癇發作,而堿中毒增強神經元興奮性和癲癇發作。
本論文研究目的是研究誘導全身性酸中毒的碳酸酐酶抑制劑(CAI)是否能阻斷窒息后癲癇發作。研究了CA抑制劑(CAIs)、乙酰唑胺(AZA)、苯甲酰胺(BZA)和乙惡唑胺(EZA)對足月出生大鼠模型中癲癇發作時對應的腦的pH值和腦P o 2的影響。
實驗步驟
用4.5%異氟醚空氣麻醉幼鼠,腹腔注射1.0 mg/g氨基甲酸乙酯,置于35℃加熱墊上。手術時異氟醚濃度降至2.5%~1.5%。將由30號針頭組成的導管連接到帶有10厘米PE10聚乙烯管并預填充0.9%NaCl的注射器,插入側尾靜脈并用氰基丙烯酸酯膠固定到位。取出一塊頭皮,在頂葉皮層兩側鉆出顱窗,使用unisense微電極系統老鼠大腦內pH值和O 2的測試(A/P-4.5,M/L 2.0 mm,距前腦門,右側pH傳感器),左側枕頂葉皮層上方,用于局部場電位(LFP)電極并在小腦(從lambda的尾部和側面約1毫米)上連接地線。在六只動物中,在下背部切開皮膚切口(長度:2-3 mm),用于測量老鼠體內的pH值和PO 2。unisense的pH(Unisense pH-500)和P o 2(Unisense OX-N)探針從麻醉后的老鼠皮膚切口推進到皮下空間至少10 mm。用細針尖小心地切開老鼠顱窗下的硬腦膜,用pH微傳感器(Unisense pH-25)、O2微電極微傳感器(Unisense OX-10)和一個玻璃毛細管LFP電極(填充溶液:150 mM NaCl)插入到大腦皮層約1 mm處,將Ag/AgCl接地線硬膜外放置在老鼠的小腦上。
實驗結果
三種CAIs可降低腦pH值0.14~0.17個pH單位,抑制窒息后癲癇電圖。AZA、BZA和EZA在脂溶性(EZA>AZA>BZA)和藥代動力學方面存在較大差異。然而,腹腔注射對腦ph的影響只有輕微的延遲(0.8-3.7分鐘)差異。CAIs誘導了窒息后腦Po2的適度升高,但對LFP活性沒有影響。AZA在行為自由的大鼠身上進行了試驗,它誘發了呼吸性酸中毒,并將驚厥發作的發生率從20只中的9只降低到17只中的2只。
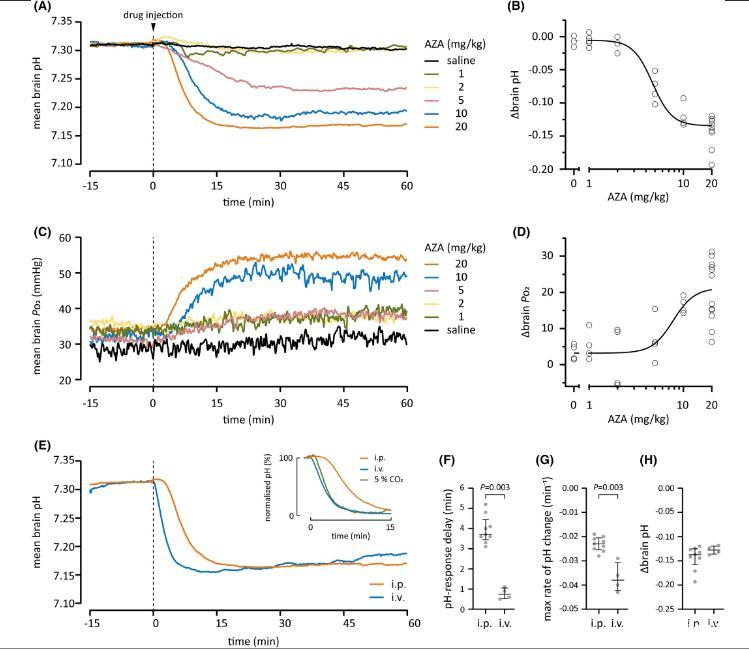
圖1、乙酰唑胺(AZA)對出生后第11天大鼠腦pH值和P o 2的影響。(A)腹膜內(ip)注射鹽水或1-20 mg/kg AZA后老鼠腦內pH值變化的時間過程和(C)P o 2顯示為連續記錄的平均值。AZA(在零時間注射)導致腦pH值降低和腦P o 2增加.(B和D):注射后45-60分鐘觀察到的AZA作用的劑量依賴性顯示20 mg/kg劑量對腦pH值的飽和作用。(E)IP和靜脈內(iv)注射20 mg/kg AZA(n=9和4)后腦pH值平均變化的時間過程。帶有歸一化y軸的插圖顯示了與吸入5%CO 2(n=5)的效果相比的相同數據。靜脈注射AZA和CO 2后腦酸中毒的發展速度相當吸入。注射AZA的延遲、最大速率和幅度。與靜脈內給藥相比,腹腔內給藥后腦pH值的下降具有較長的發作延遲,定義為從注射到最大變化的10%(F)的時間,并且以較低的速率(G)發生。(H)兩種給藥途徑在注射后45-60分鐘的腦pH值沒有差異。(FH)中的條形表示中位數和四分位距。
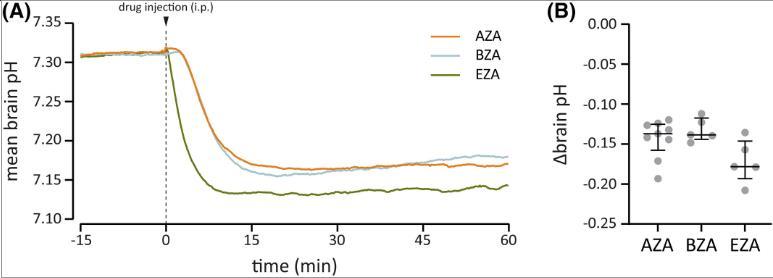
圖2、碳酸酐酶抑制劑乙酰唑胺(AZA)、苯甲酰胺(BZA)和乙惡唑胺(EZA)對腦pH值的影響。(A)腹腔(ip)注射20 mg/kg AZA或等摩爾劑量(90μmol/kg)BZA或EZA后腦pH值平均變化的時間過程。與AZA或BZA相比,注射EZA后腦pH值下降得更快。注射后45-60分鐘記錄的腦pH變化幅度(B)在藥物之間沒有差異。(B)中的條形表示中位數和四分位數范圍。
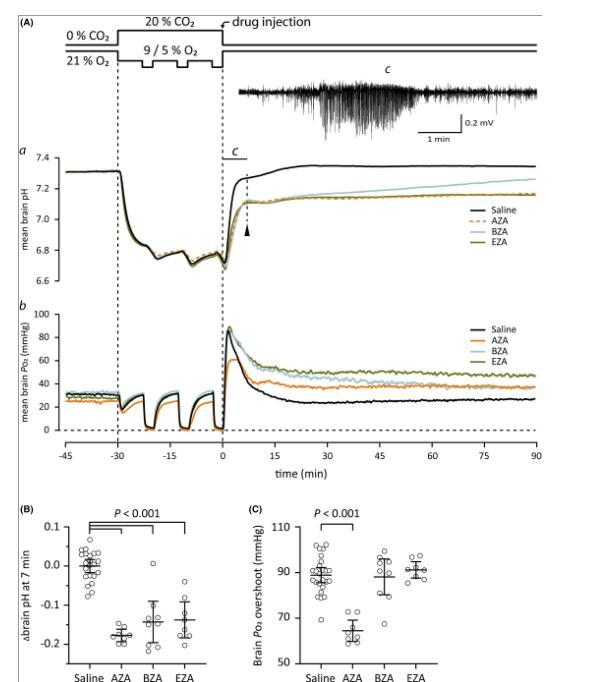
圖3、碳酸酐酶抑制劑(CAIs)乙酰唑胺(AZA)、苯甲酰胺(BZA)和乙惡唑胺(EZA)對窒息后老鼠腦內pH值和Po 2的影響。(A)頂部的線圖顯示了窒息后恢復開始時的氣體應用方案和靜脈注射藥物(90μmol/kg)的時間。垂直虛線標記窒息的開始和結束。窒息結束時,腦pH(a)嚴重酸中毒,腦P o 2(b)幾乎為零。恢復室內空氣后,大腦pH值快速增加7分鐘(快速恢復階段結束,用箭頭標記)之后慢慢穩定在基線水平附近。Brain P o 2超過基線水平,隨后迅速恢復至基線。癲癇發作總是出現在大腦pH值恢復的快速階段。插圖(c)中顯示了在這7分鐘期間內注射鹽水的大鼠中記錄的樣本局部場電位。快速pH恢復階段(7分鐘)結束時的腦pH值顯示在B中。鹽組平均pH值已從值中扣除。用任何CAI治療的動物的腦pH值較低。(C)腦P o 2在過沖的峰值。

圖4、乙酰唑胺(AZA)可抑制窒息后驚厥發作。自由活動大鼠中陣攣和/或強直陣攣窒息后癲癇發作的發生率(A)和持續時間(B)。窒息結束前10分鐘腹腔給予20mg/kg AZA或生理鹽水。
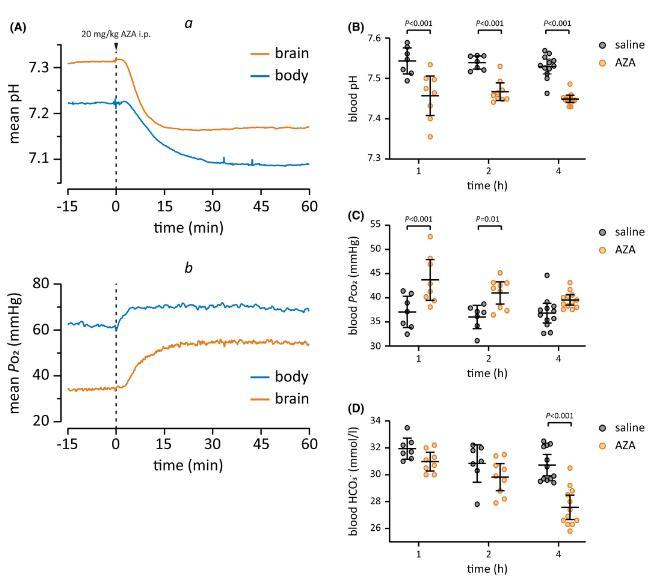
圖5、乙酰唑胺(AZA)可誘導快速、短暫的呼吸性酸中毒和延遲性代謝性酸中毒。(A)腹膜內(ip)注射20 mg/kg AZA后皮下(“身體”)和腦pH(a)和P o 2(b)變化的時間過程,顯示為連續記錄的平均值(n=5代表身體,12代表大腦記錄)。在基線期間,身體pH值略低,P o 2遠高于大腦。AZA注射后身體和大腦的pH值降低了相似的量。P o 2的平行增加在大腦中比在身體中更為突出。血液pH(B),Pco 2(C)和HCO3-濃度(D)腹腔注射20 mg/kg AZA后1-4小時(2小時第二次給藥)。
結論與展望
本論文研究了CA抑制劑(CAIs)、乙酰唑胺(AZA)、苯唑胺(BZA)和乙氧唑胺(EZA)對足月窒息大鼠癲癇發作、腦pH和腦Po2的影響。研究表明CAIs以類似于外源性CO 2的方式抑制出生窒息大鼠模型中的癲癇發作。24在臨床上使用易于給藥的藥物顯然比使用5%CO2吸入要簡單得多。現在判斷哪種特定的CAI藥物在治療新生兒窒息后癲癇發作中是最佳的(參見30)還為時過早。然而,現有的臨床數據表明AZA在新生兒和兒科人群中具有很高的安全性和耐受性,這表明這種抗癲癇藥物可用于NICU。AZA、BZA和EZA可有效阻斷窒息后癲癇發作。盡管它們的藥代動力學存在差異,但它們對腦pH值的影響相似,這表明它們的抗癲癇作用模式是基于抑制血源性和細胞外血管碳酸酐酶導致的呼吸性(高碳酸血癥)酸中毒。AZA已被用于新生兒的多種適應癥,這表明它可以安全地重新用于治療新生兒癲癇發作,作為當前治療方案的補充。