熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
研究簡介:鐵是地殼中最豐富的氧化還原活性元素。硝化-還原鐵(II)-氧化細菌已經知道大約20年了。在多大程度上降低硝酸鹽和鐵的氧化是通過酶的途徑或由異養反硝化形成的亞硝酸鹽引起的非生物過程這個結論,已經引起了許多爭論。到目前為止,唯一已知的實驗室可以長期維持培養的是culture KS,這種純具有自養硝酸鹽還原Fe(II)氧化能力的培養物,然而能夠連續Fe(II)氧化和自養的能力的微生物代近些年來還未培養出來,只是在近幾年在沿海海洋沉積物中,還發現了自養硝酸鹽還原鐵(II)-氧化細菌的存在。
本論文研究的目的是通過監測底物濃度和活性的變化來評估硝酸鹽還原和鐵(II)氧化的耦合,以及對天然淺海淡水沉積物中的硝化細菌的活性對硝酸鹽和鐵的刺激(II)的影響。
Unisense微電極系統的應用
應用了溶氧微電極OX-100,氧化還原電極以及PH-100三種微電極對康斯坦斯湖沿岸所取的沉積物柱芯樣品的氧、pH、氧化還原電位等進行了原位測試,其中對在所取的沉積物測量之前和測試期間,在沉積物中覆蓋的水進行曝氣,這是為了還原海洋種的表面沉積物中是充滿了氧氣的。對于沉積物中的氧的微剖面測試采用的是手動微推進器,每次測試步徑為200微米。而對于氧化還原電位以及pH的微剖面測試采用的測試步徑是500微米。
實驗結果
研究發現在經過改良的微生態系統中。鐵的生物氧化依賴于微生物同步還原硝酸的過程,此外還發現亞硝酸鹽在經過消毒的沉積物中,亞硝酸鹽的非生物氧化反應速度不足以解釋在微生物活性沉積物中觀察到的鐵氧化速率。此外酶的基因編碼的表達水平對硝酸鹽還原至關重要,尤其受到了環境中二價鐵的刺激作用。這些結果表明,二價鐵對細菌的反硝化作用有直接的影響,并支持了微生物硝酸鹽的減少是由生物鐵(II)氧化引起的的假說。
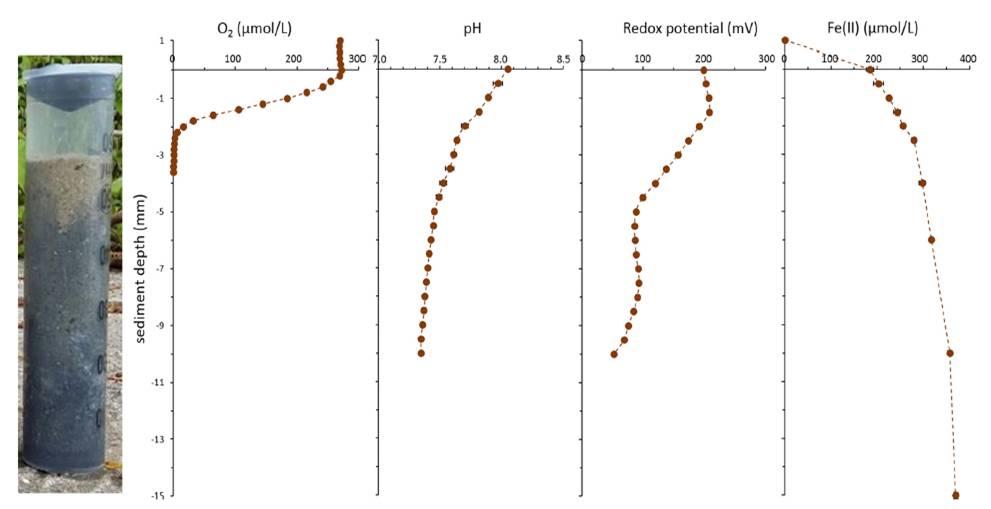
圖1、康斯坦斯湖沿岸沉積巖心中測試的氧,pH,氧化還原電位,和Fe(II)的剖面圖。從圖中可以看出,所取的海洋沉積物中的氧的濃度是隨著距離界面越遠,其氧的濃度最近降低,大約在界面下4mm處體系中的氧濃度幾乎為零。對于沉積物巖心中的pH值也是隨著沉積物界面處的深度增加表現為不斷變小。而對于氧化還原電位值表現為先減小后并最后穩定120mv,但是體系中的二價鐵則表現為隨著距離沉積物界面處的距離增加,其二價鐵的濃度逐步增加。
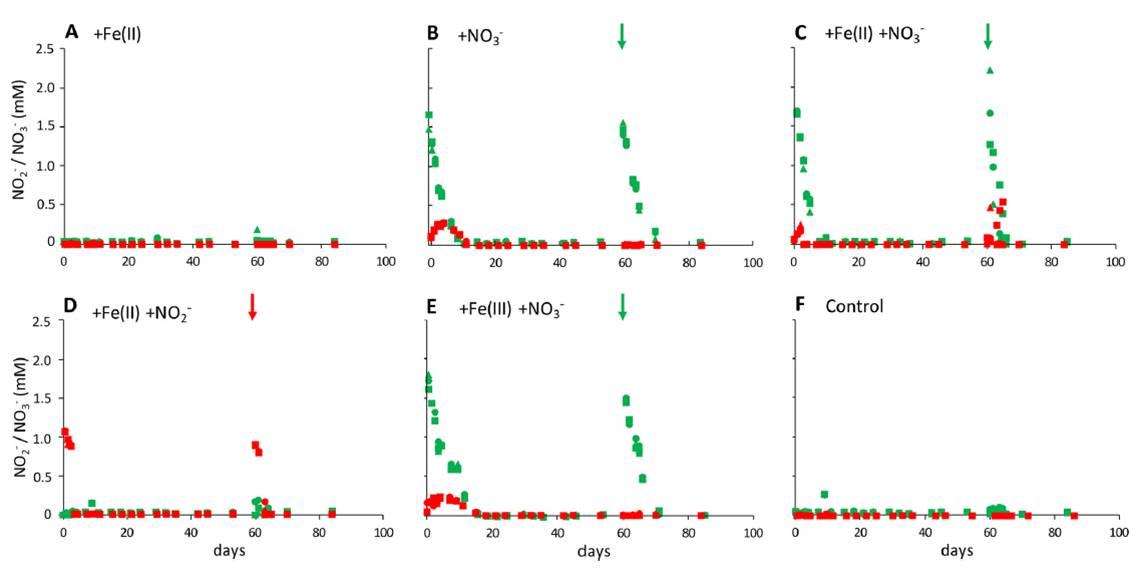
圖2、在不同的微觀環境中測試的硝酸鹽(綠色)和亞硝酸鹽(紅色)的濃度(三角形、正方形和菱形符號分別代表了三倍體系的濃度)。體系中更正的濃度(5 mM的Fe(II)和Fe(III)除了從沉積物中衍生出1mM,2mM來自于硝酸鹽和亞硝酸鹽),微觀環境的加入表示的是加入硝酸鹽或亞硝酸鹽后第60天。
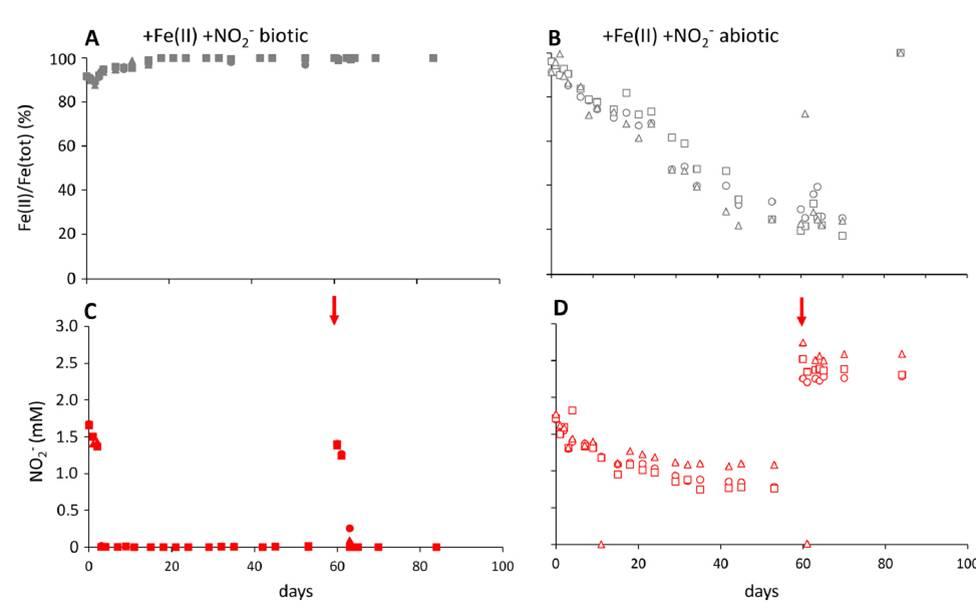
圖3、亞硝酸鹽濃度(紅色)和Fe(II)/Fe(tot)比率(灰色)在生物(填充的符號)和非生物(空心結構符號)隨著時間的變化情況(三角形,正方形,和鉆石符號顯示的三倍體系)。其中在初始修正后的Fe[II]濃度為5 mM,亞硝酸鹽濃度為2 mM,微觀體在第60天(見箭頭)加入亞硝酸鹽后呈現的體系濃度情況。
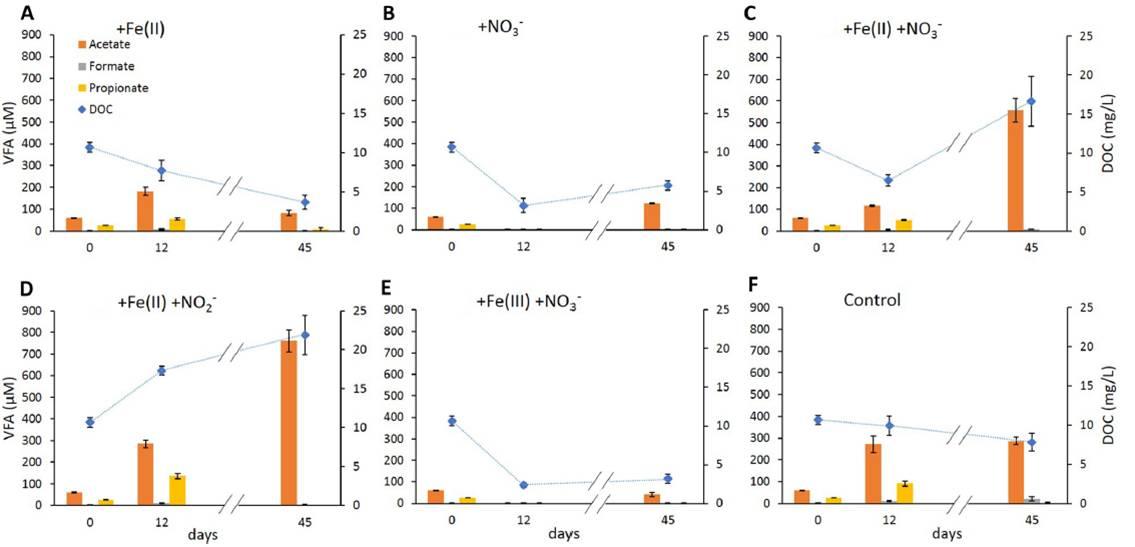
圖4、隨著時間的推移,體系中溶解的有機碳(藍色鉆石符號)和揮發性脂肪酸(棒)的濃度在設置的不同微觀環境體系中隨時間的變化情況。
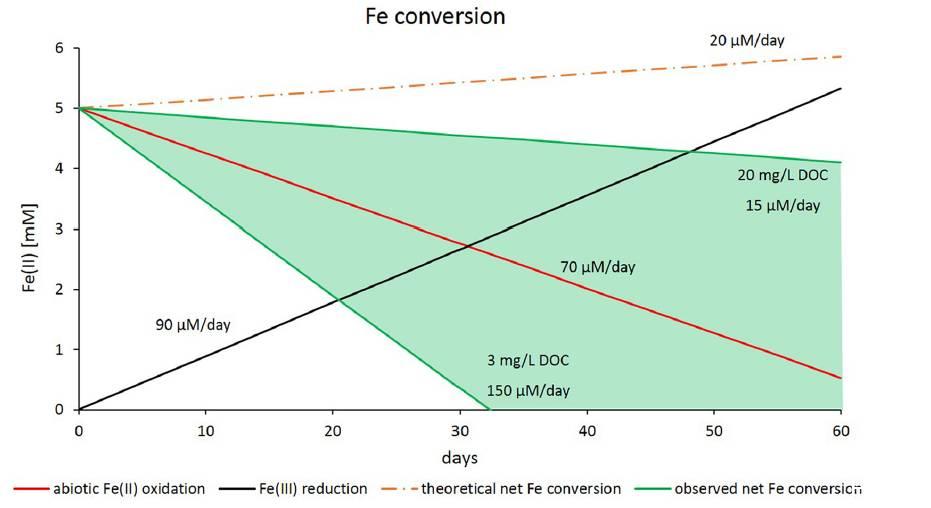
圖5、鐵的轉化率(同步顯示的凈利率,其中Fe[II]氧化和Fe[III]的還原都依賴于DOC的濃度。選用5mM的Fe(II)或Fe(III)和2mM的硝酸鹽或亞硝酸鹽進行的微觀實驗的相關測試。理論鐵的轉換率顯示了Fe(II)的氧化反應只與亞硝酸鹽的反應有關的假設。理論Fe的轉換率(橙色虛線)與實測Fe的轉化率區別。
總結
本論文主要就沿海沉積物中的Fe(II)氧化與硝酸鹽還原進行相關研究,之前的很多研究認為,沉積物中的Fe(II)氧化對硝酸鹽還原的依賴性導致了兩個過程都是酶耦合的結論,但是結合實際觀察卻發現,普通的硝酸鹽還原菌可以通過反應性氮素,在非生物的條件下氧化Fe(II)。在反硝化過程中觀察到的這些結果引起了相關科研人員對于體系中的硝酸鹽還原與Fe(II)氧化的耦合酶是否存在產生懷疑,本論文基于此項研究的疑慮,結合使用了unisense微電極研究系統實現了原位的測試沉積物中的Fe(II)、氧氣、pH、氧化還原電位等相關參數,提出了沉積物中硝酸還原鐵(II)氧化的基本機理,并且得出了Fe(II)氧化與硝酸鹽還原反應主要是一種微生物介導的過程。這說明微電極在研究海洋沉積物氮循環機理方面存在著非常好的應用前景。
 相關新聞
相關新聞