熱線:021-66110819,13564362870
Email:info@vizai.cn


熱線:021-66110819,13564362870
Email:info@vizai.cn
吳一戎院士(中國(guó)科學(xué)院空天信息創(chuàng)新研究院)新綜述介紹了腦類器官的最新模型進(jìn)展,它為神經(jīng)科學(xué)和疾病建模領(lǐng)域的研究提供了深入的見解和創(chuàng)新方法。文章首先指出,目前人類神經(jīng)疾病模型的建立采用的是體內(nèi)和體外動(dòng)物模型。但是,由于動(dòng)物模型無(wú)法準(zhǔn)確復(fù)制人類生理,大約只有三分之一的動(dòng)物模型能為人類臨床試驗(yàn)提供可靠的支持或有效轉(zhuǎn)化。
因此,急需能夠準(zhǔn)確模擬人類生理的神經(jīng)病病模型。幸運(yùn)的是,人誘導(dǎo)多能干細(xì)胞(hiPSCs)技術(shù)為體外重現(xiàn)人類生理和微環(huán)境提供了新的研究可能性,特別是通過(guò)發(fā)展干細(xì)胞衍生的器官芯片。文章深入探討了使用人誘導(dǎo)多能干細(xì)胞衍生神經(jīng)元(hiPSC-DNs)建立的體外神經(jīng)病模型的重要性。
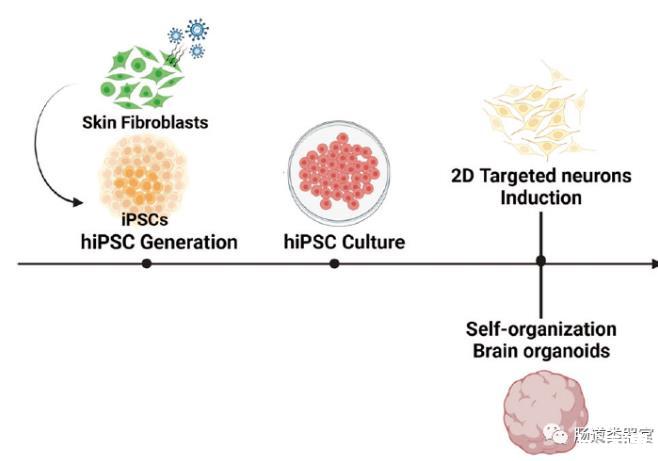
基于3D人腦類器官模型的轉(zhuǎn)錄組分析發(fā)現(xiàn),PCCB敲低主要導(dǎo)致了γ-氨基丁酸(GABA)信號(hào)通路障礙。進(jìn)一步的代謝組學(xué)分析、ELISA等實(shí)驗(yàn)發(fā)現(xiàn),PCCB敲低抑制了三羧酸(TCA)循環(huán)關(guān)鍵中間產(chǎn)物α-酮戊二酸、琥珀酰輔酶A和琥珀酸鹽的合成,不僅導(dǎo)致了線粒體ATP合成減少、活性氧水平增高,還降低了細(xì)胞中GABA的含量。微電極陣列(MEA)電生理檢測(cè)發(fā)現(xiàn),PCCB敲低導(dǎo)致類腦器官的放電頻率增高、同步性降低,表明類腦器官的突觸功能和神經(jīng)網(wǎng)絡(luò)連接出現(xiàn)障礙。在PCCB敲低的類腦器官培養(yǎng)液中添加外源性α-酮戊二酸可以挽救TCA循環(huán)中間產(chǎn)物和GABA含量的減少,表明PCCB通過(guò)TCA循環(huán)途徑發(fā)揮作用。
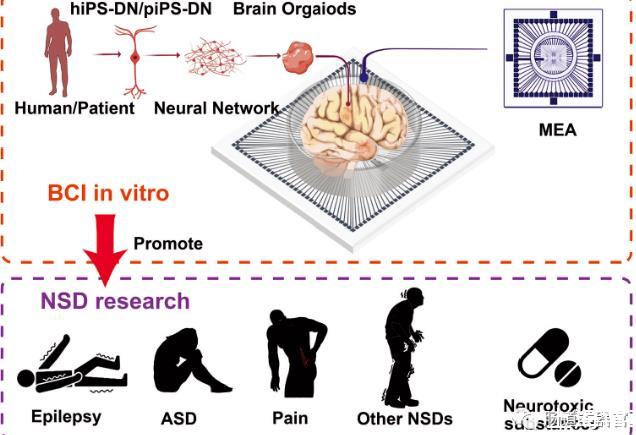
這些模型使用微電極陣列(MEAs)與二維和三維的神經(jīng)干細(xì)胞衍生體外模型界面,以實(shí)時(shí)監(jiān)測(cè)它們的生理活動(dòng)。因此,MEAs成為使用人類iPSCs體外模擬神經(jīng)障礙和疾病的新興和有用工具。這篇綜述詳細(xì)介紹了MEA在分析hiPSC-DNs建立的神經(jīng)疾病模型中的作用,涵蓋了MEA的制造、表面結(jié)構(gòu)、修飾方案、hiPSC-DNs的培養(yǎng)和信號(hào)檢測(cè)的重要性。
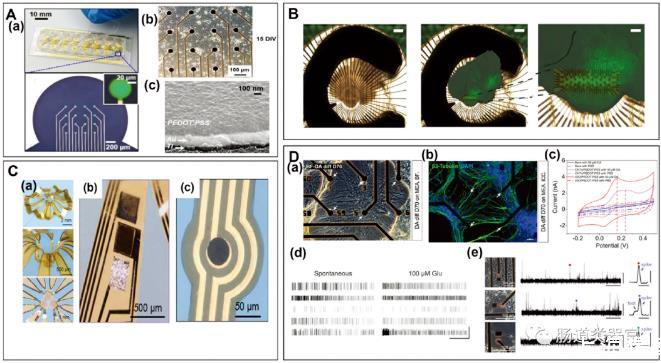
此外,還討論了MEA技術(shù)在研究體外神經(jīng)疾病模型(包括癲癇、自閉癥譜系發(fā)育障礙(ASD)等)的進(jìn)展,以及hiPSC-DNs結(jié)合MEA檢測(cè)體外神經(jīng)毒性物質(zhì)的應(yīng)用。
最后,文章還探討了多功能集成設(shè)備在體外醫(yī)療診斷和治療方面的未來(lái)發(fā)展和展望。這篇文章是對(duì)于神經(jīng)科學(xué)研究者和臨床醫(yī)生來(lái)說(shuō),尤其是那些對(duì)神經(jīng)疾病建模和干細(xì)胞技術(shù)感興趣的人,是一篇不可錯(cuò)過(guò)的重要文獻(xiàn)。它不僅提供了當(dāng)前該領(lǐng)域的全面回顧,還為未來(lái)的研究方向和應(yīng)用提供了寶貴的洞見。
 相關(guān)新聞
相關(guān)新聞